Formación de la banda mediante el solapamiento orbital.
El solapamiento de un gran número de orbitales atómicos conduce a un conjunto de orbitales moleculares que se encuentran muy próximos en energías y que forman virtualmente lo que se conoce como una banda. Las bandas se encuentran separadas entre sí mediante espacios energéticos a los que no les corresponde ningún orbital molecular (Figura 2).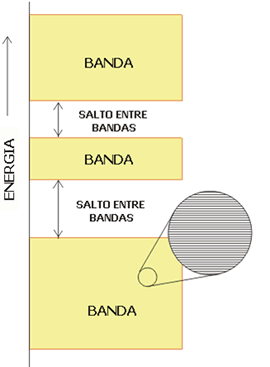
Figura 2. La estructura electrónica de un sólido se caracteriza por la existencia de bandas de orbitales.
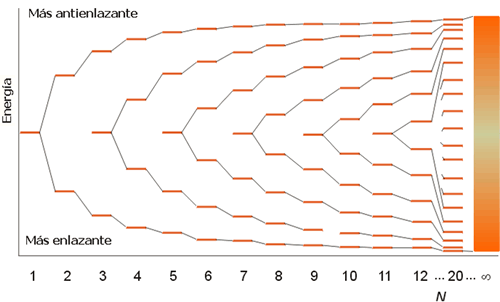
Figura 3. Formación de una banda de orbitales moleculares.
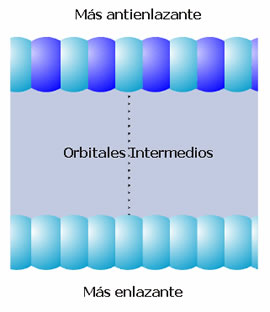
Figura 4. Orbitales moleculares y banda s.
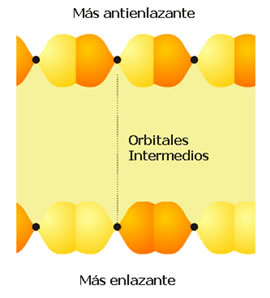
Figura 5. Orbitales moleculares y banda p.
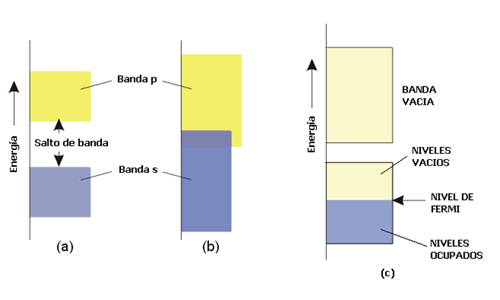
Figura 6. (a) y (b) Bandas s y p, que pueden solapar o no, dependiendo de la anchura. (c) Niveles ocupados y nivel de Fermi a o K.
El nivel de Fermi
A la temperatura T = 0 K los electrones ocupan los orbitales moleculares que forman la banda siguiendo el principio de construcción citado en la lección 2. Si cada átomo del modelo (distribución lineal de átomos) contribuye a la banda s con 1 electrón entonces, a T = 0 K la mitad de los orbitales que forman la banda (1/2 N) estarán ocupados. El orbital molecular de mayor energía que se encuentra ocupado se conoce como el nivel de Fermi y, en este caso, estará situado en el centro de la banda. La banda de menor energía que se encuentra ocupada o semiocupada se conoce como banda de valencia. La banda de menor energía que se encuentra vacía se conoce como la banda de conducción.A una temperatura superior a 0 K, la población de los orbitales moleculares que forman la banda, P, viene dada por la distribución de Fermi-Dirac, que es una versión de la distribución de Boltzmann, y que tiene en cuenta que cada nivel de energía de la banda sólo puede estar ocupado por 2 electrones como máximo. Esta distribución P tiene la siguiente forma:
P = 1/(e(E-μ)/kT + 1)
donde μ es el potencial químico o energía del nivel para el cual P = 1/2. La forma de la distribución de Fermi-Dirac se muestra en la Figura 7. Cuando la banda no está completamente ocupada los electrones que se encuentran próximos al nivel de Fermi pueden, fácilmente, promocionarse a niveles vacíos que se encuentran inmediatamente por encima de éste. Como resultado, los electrones gozan de movilidad y pueden moverse libremente a través del sólido. Este fenómeno origina que la sustancia sea un buen conductor eléctrico. Como se ha visto, en un metal la conductividad eléctrica disminuye con la temperatura; este hecho se debe a las interferencias (los electrones se pueden describir como ondas) que se producen entre los electrones que se mueven por el sólido y las vibraciones de la red cristalinas, provocadas por el movimiento de los átomos, vibraciones que aumentan al hacerlo la temperatura. La densidad de estados.
El número de niveles de energía con un determinado valor de energía se conoce como la densidad de estados, N(E) o ρ. Es posible representar la variación de energía de una banda en función de la densidad de estados, tal como aparece en la Figura 8 para las bandas s y p. La densidad de estados no es uniforme a lo largo de toda la banda debido a que los niveles de energía se empaquetan más a unos determinados valores de energía que a otros. Este hecho produce que la banda s, por ejemplo, presente la mayor densidad de estados en el centro y la menor densidad de estados en los extremos de la banda. La razón de este comportamiento está en la forma de las combinaciones lineales que originan los orbitales moleculares que constituyen la banda s. Existe una única combinación lineal que conduce al orbital molecular más enlazante (el límite inferior de la banda)y otra que conduce al más antienlazante (el límite energético superior de la banda). Sin embargo hay varias combinaciones posibles, degeneradas en energía, que dan lugar a los orbitales moleculares que forman la parte central de la banda s.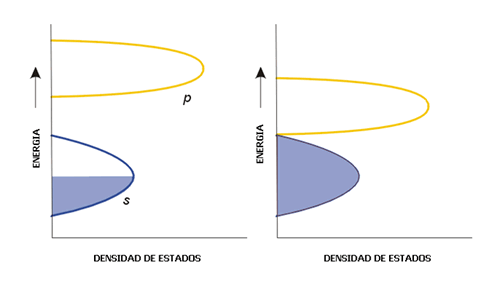
Figura 8. Densidad de estados típica de un metal (izquierda) y de un semimetal (derecha).
Nombre: Luiggi D. Escalante Sarmiento
CI. 18.878.611
Materia: EES
Fuente: http://www.textoscientificos.com/quimica/inorganica/enlace-metales/teoria-bandas
GRACIAS❤
ResponderEliminar